 |
 |
||
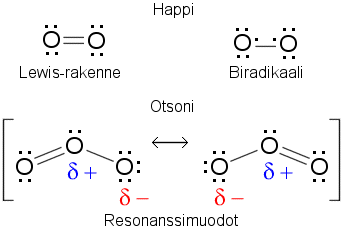
| Happi | Otsoni | Rakennekaavat | |
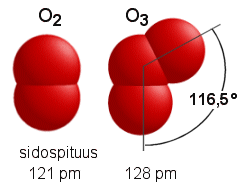
Happi ja otsoni ovat alkuainehapen allotrooppisia muotoja. Hapen kolmantena allotrooppina voidaan pitää atomaarista happea (O), jota esiintyy luonnossa mm. stratosfäärissä. Happi O2 on kaasuna hajutonta ja väritöntä, nesteenä vaaleansinistä. Happi on paramagneettista (nesteenä se tarttuu vahvan magneetin napoihin). Otsoni O3 on kaasuna pistävänhajuista ja vaalean sinertävää, nesteenä voimakkaan sinistä. Otsoni on diamagneettista. Otsoni on myrkyllistä.
Suurin osa ilmakehän otsonista, yli 90 %, on stratosfäärissä 15 km:n korkeudelta alkavassa, liki 20 km:n paksuisessa ilmakerroksessa. Kerroksen otsonipitoisuus on suurimmillaan 25 km:n korkeudessa. Jos stratosfäärin otsoni puristettaisiin maan pinnalla vallitsevaan paineeseen yhtenäiseksi kerrokseksi 15 °C lämpötilassa, kerroksen vahvuudeksi tulisi vain 2 – 4 mm, kun koko ilmakehälle paksuutta kertyisi 8,4 km.
Stratosfäärin otsonimäärät on tapana ilmoittaa Dobson-yksikköinä (DU), jotka kuvaavat ns. lasketun otsonikerroksen paksuutta. Otsonikerros, jonka paksuus olisi 1,00 mm 1,013 barin paineessa ja 15 °C:n lämpötilassa, vastaa otsonimäärältään 100 Dobson-yksikköä. Normaalit otsonipitoisuudet ovat pohjoisella pallonpuoliskolla 300 – 430 DU, tropiikissa keskimäärin 260 DU ja Australiassa 280 – 360 DU.
Nykyisin (1990- luvulla ja vuosituhannen vaihteen tienoilla) otsonin kokonaismäärä alenee keväisin liki 150 DU-yksikköön. Ohuimmillaan Etelämantereen otsonikerros oli lokakuussa 1987, jolloin englantilaisella Scottin tutkimusasemalla mitattiin lukemaksi 140 DU-yksikköä.
Maapallon elämälle otsonikerros on välttämätön, sillä se suojaa eläviä soluja vaaralliselta ultraviolettisäteilyltä. Säteilyn sitoutuminen eli absorptio on normaalissa otsonikerroksessa niin tehokasta, että vain yksi 30 000 000:s osa auringon UV-säteilystä pääsee kerroksen läpi. Sitoutuminen perustuu siihen, että UV-säteily hajottaa stratosfäärissä sekä O2- että O3-molekyylejä. Hajoamistuotteista muodostuu kuitenkin uudelleen O3-molekyylejä.
Säteilyn ohella vapaat happiatomit hajottavat hitaasti otsonia. Tässä luonnollisessa kierrossa otsonin määrä vaihtelee jonkin verran sekä leveysasteen että vuodenajan mukaan, ts. auringon säteilyn voimakkuuden mukaisesti. Esimerkiksi pohjoisella pallonpuoliskolla otsonia on tavallisesti eniten huhtikuussa ja vähiten lokakuussa. 1990- luvulla ja vuosituhannen vaihteen tienoilla Etelämantereen ja Pohjoismaiden yläpuolella on havaittu otsonipitoisuuksien pudonneen jopa 40 % pitkäaikaisista keskiarvoista. Tätä otsonikatoa ei voida selittää pelkän luonnollisen vaihtelun perusteella. Pääasiallisena syynä ovat ilmaan päästetyt halogenoidut hiilivedyt, kuten CFC-aineet ja halonit. Lisäksi ilmakehän ydinräjäytykset, yliäänikoneiden ja avaruuslentojen päästöt vähentävät otsonin määrää.
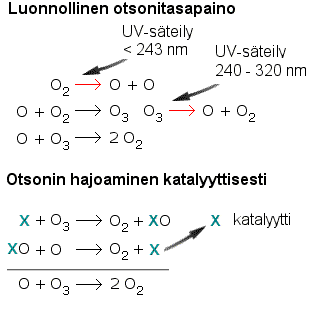 |
UV-säteilyä hajottaa sekä happimolekyylejä että otsonimolekyylejä. Näissä reaktioissa UV-säteilyä siis sitoutuu. Happiatomit hajottavat otsonimolekyylejä. Tämä reaktio nopeutuu katalyytin vaikutuksesta .Katalyytti X voi olla voi olla H, OH, NO, Cl tai Br. Katalysoidussa reaktiossa UV-säteilyä ei sitoudu. |
Otsonin hajoamista katalysoivia aineita tulee ilmakehään myös luonnon päästölähteistä ja prosesseista. Auringon purkauksissa vapautuu elektroneja ja protoneja, joilla on suuri energia. Osa niistä iskeytyy maan ilmakehään ja osuu etupäässä napa-alueille. Ilmakehässä protonit ja elektronit ionisoivat ja pilkkovat molekyylejä. Näin muodostuu mm. OH-radikaaleja ja NO-molekyylejä, jotka katalysoivat otsonin hajoamisreaktiota. Tulivuorenpurkauksissa vapautuu myös joitakin katalysoivia yhdisteitä (mm. HCl), mutta ei ole varmaa, pääsevätkö ne vaikuttamaan stratosfääriin asti. Ihmisten tuottamien otsonikerrosta ohentavien aineiden osuudeksi arvioidaankin 80 – 85 %, mutta luonnon omien prosessien osuutta ei kylläkään vielä täysin tunneta.
| Eräitä tavallisia CFC-aineita ja halogeenihiilivetyjä | Elinikä a | |||
| Nimi | Kaava | Käyttö | ilmakehässä | ODP* |
| CFC-11 | CFCl3 | Ponnekaasuna ja muovien vaahdotuksessa | 45 | 1,0 |
| CFC-12 | CF2Cl2 | Jäähdytys- ja lämpöpumppulaitteissa | 100 | 1,0 |
| CFC-113 | C2F3Cl3 | Pesuaineena ja rasvan liuottimena | 85 | 0,8 |
| CFC-114 | C2F4Cl2 | Ponnekaasuna, muovien vaahdotuksessa, sammuttimissa, rasvan liuottimena, rähähteiden valmistuksessa | 300 | 1,0 |
| CFC-115 | C2F5Cl | Epäorgaanisten pigmenttien sekä eräiden kemikaalien, muovien, hartsien ja pinta-aktiivisten aineiden valmistuksessa | 1700 | 0,6 |
| Halon 1211 | CF2ClBr | Sammuttimissa | 16 | 3 |
| Metyylibromidi | CH3Br | Kasvinsuojeluaineena | 0,7 | 0,6 |
| Hiilitetrakloridi | CCl4 | Liuottimena | 26 | 1,1 |
| *ODP ozone depletion potential, Montrealin pöytäkirjan mukaan. Arviot vaihtelevat. Yhdisteet ovat myös kasvihuonekaasuja. Taulukon useimpia yhdisteitä ei enää käytetä Montrealin sopimusmaissa.Tilalle on kehitetty korvaavia aineita ja prosesseja. | ||||
Lisää tietoa taulukoituna: Ozone-Depleting Substances, EPA (USA)
Koska ODP-aineet ovat katalyyttejä ja erittäin pitkään ilmakehässä säilyviä, niiden käytön lopettaminen ei vaikuta heti otsonikerroksen tilaan. Mikäli sopimukset käyttörajoituksista pitävät, odotetaan otsonikerroksen palautuvan ennalleen aikaisintaan 2050-luvulla.
Kemian Nobel 1995 otsonitutkijoille
Montrealin sopimus (Montreal Protocol), joka syntyi vuosina 1985-1987, on useiden valtioiden (136) ratifioima asiakirja, jossa on sovittu eräiden otsonikerrosta tuhoavien aineiden käytön rajoittamisesta tai lopettamisesta. Allekirjoittajamaiden joukkoon kuuluvat lähes kaikki teollistuneet valtiot. Ensimmäinen seurantakokous pidettiin Helsingissä 2.- 5. toukokuuta 1989. Sopimuksessa on mainittu CFC-aineet, halonit ja metyylibromidi. Sopimuksen päätavoitteena on estää ihmistoiminnan aiheuttama otsonikerroksen tuho. Toisena tavoitteena on tukea ja koordinoida asiaan liittyvää tutkimusta.
Why
Does The Ozone Hole Form? Beloit College , University of
California
osa Chem Connections Modules -oppimateriaalista, joka
sisältää mm. QuickTime-esityksiä ja -videoita, runsaasti
linkkejä
Otsonia kuluttavat aineet:
http://chemistry.beloit.edu/Ozone/pages/molecule.html