| Yhdiste | C2H2 | C3H8 | CH3OH | HCOOH | CH3OCH3 | |
| Hiilivety | ||||||
| Tyydyttymätön yhdiste |
||||||
| Poolinen molekyyli |
||||||
| Vetysidoksia molekyylien välillä |
||||||
| Hapan vesiliuos |
Oheisessa taulukossa on esitetty joitakin yhdisteitä ja niihin mahdollisesti liittyviä ominaisuuksia. Kopioi alla oleva taulukko vastauspaperiisi ja vastaa "kyllä" tai "ei" taulukon avoimiin kohtiin
| Yhdiste | C2H2 | C3H8 | CH3OH | HCOOH | CH3OCH3 | |
| Hiilivety | ||||||
| Tyydyttymätön yhdiste |
||||||
| Poolinen molekyyli |
||||||
| Vetysidoksia molekyylien välillä |
||||||
| Hapan vesiliuos |
Ureaa, (NH2)2CO, voidaan valmistaa ammoniakin ja hiilidioksidin välisessä reaktiossa, jolloin tuotteena urean ohella saadaan vettä.
| a) | Laadi reaktion yhtälö. (2 p.) |
| b) | Kuinka monta grammaa ureaa voidaan saada, kun lähtöaineina käytetään 637 g ammoniakkia ja 1140 g hiilidioksidia? (4 p.) |
Paineen kestävässä astiassa sytytetään kaasuseos, jossa on 50 ml etaania ja 520 ml happea sekä 70 ml erästä alkeenia, CnH2n. Täydellisen palamisen jälkeen astiassa on 30 ml reagoimatonta happea. Mikä on alkeenin molekyylikaava? Kaikki tilavuudet on ilmoitettu samoissa olosuhteissa.
Kuvassa on esitetty kahden aminohapon, alaniinin ja isoleusiinin, rakennekaavat.
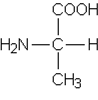 |
 |
| alaniini | isoleusiini |
| a) | Kiinteää alaniinia liuotetaan natriumhydroksidin vesiliuokseen. Laadi reaktion yhtälö. (2 p.) |
| b) | Kun kaksi aminohappomolekyyliä reagoi keskenään, muodostuu dipeptidi. Esitä alaniinin ja isoleusiinin välisessä reaktiossa syntyvien dipeptidien rakennekaavat. (4 p.) |
0,50 litrassa liuosta on 1,0 millimoolia suolahappoa
(vetykloridia) lämpötilassa
| a) | Mikä on liuoksen pH? (1 p.) |
| b) | Mihin tilavuuteen liuos on laimennettava, jotta sen pH olisi 3,00? (2 p.) |
| c) | Kuinka suuri tilavuus 0,10 M NaOH-liuosta on lisättävä alkuperäiseen suolahappoliuokseen, jotta muodostuvan liuoksen pH olisi 12,00? (3 p.) |
Tarkastele seuraavia orgaanisia yhdisteitä: A CH3CH2CH(CH3)CHCH2, B CH3NH2, C CH3CH2COOH
| a) | Yhdiste A on molekyylissä olevan asymmetrisen (kiraalisen) hiiliatomin takia optisesti aktiivinen. Merkitse asymmetrinen hiiliatomi yhdisteen rakennekaavaan tähdellä (1 p.) |
| b) | Yhdistettä A valmistetaan synteettisesti. Miksi tuote ei ole optisesti aktiivinen? (2 p.) |
| c) | Esiintyykö yhdisteellä A cis-trans-isomeriaa)? Perustele. (1 p.) |
| d) | Laadi rakennekaavoja käyttäen yhdisteen B ja C välisen reaktion yhtälö. (2 p.) |
Aineen ominaisuudet johtuvat ensisijaisesti aineessa esiintyvistä kemiallisista sidoksista. Selvitä sidosten avulla, miksi
| a) | metallit johtavat sähköä, (2 p.) |
| b) | jalokaasuilla on alhainen kiehumispiste, (2 p.) |
| c) | suolat liukenevat veteen. (2 p.) |
Selvitä, miksi
| a) | olut kuohuu pulloa avattaessa, (2 p.) |
| b) | avoimessa pullossa viini happanee helposti, (2 p.) |
| c) | kananmunan valkuainen hyytyy keitettäessä. (2 p.) |
Alla on kuvattu eräiden atomien kokoa. Mistä atomien erilainen koko johtuu? Millainen on kationien ja anionien koko verrattuna saman varauksettoman atomin kokoon?
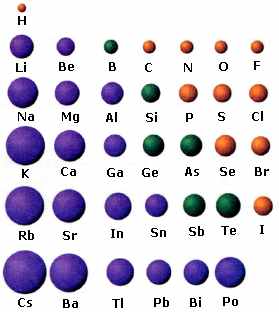
Analysoitava valkoinen jauhe saattoi olla joko kaliumkloridia, kaliumfluoridia tai kaliumkarbonaattia. Kun jauheesta otettu pieni näyte liuotettiin veteen, todettiin liuoksen kastetun lakmuspaperin värjäytyvän siniseksi. Mitään näkyvää reaktiota ei tapahtunut, kun liuokseen lisättiin suolahappoa. Mikä valkoinen jauhe oli? Perustele valintasi.

Autojen pakokaasut sisältävät ympäristölle haitallisia kaasuja, kuten hiilivetyjä, typpimonoksidia ja hiilimonoksidia. Ne voidaan kuitenkin pääosin muuttaa pakokaasukatalysaattorin avulla ympäristölle vähemmän haitallisiksi yhdisteiksi.
| a) | Pohdi, mitä ympäristöhaittoja aiheutuu edellä mainituista yhdisteistä, jos ne joutuvat ilmaan sellaisinaan. (5 p.) |
| b) | Mihin pakokaasukatalysaattorin toiminta perustuu? Kirjoita mahdolliset reaktioyhtälöt. (4 p.) |
Reaktion
tasapainovakio määritettiin seuraavalla tavalla. Eri määrät vetyjodidia suljettiin viiteen 0,400 litran astiaan, joita säilytettiin lämpötilassa 623 K. Tietyn ajan kuluttua astiat avattiin ja muodostunut jodi määritettiin titraamalla 0,0150 M natriumtiosulfaatilla reaktion
mukaisesti. Määritä näin saatujen kokeellisten tulosten perusteella reaktion tasapainovakion arvo. Mitkä seikat vaikuttavat tuloksen luotettavuuteen?
| Reaktioastian
numero |
HI(g):n
alkuperäinen määrä grammoina |
Astian
avaamisaika reaktion alusta lukien tunteina |
Titrauksessa
kuluneen tiosulfaatin tilavuus millilitroina |
| 1 | 0,300 | 2 | 20,96 |
| 2 | 0,320 | 4 | 27,90 |
| 3 | 0,315 | 12 | 32,31 |
| 4 | 0,406 | 20 | 41,50 |
| 5 | 0,280 | 40 | 28,68 |