Valitse kolme kohtaa seuraavasta luettelosta ja selvitä näiden kemiallinen perusta:
Auton bensiinin kulutus on 7,9 l/100 km. Kuinka suuri tilavuus hiilidioksidia lämpötilassa 25 °C ja paineessa 1,0 bar (=100 kPa) muodostuu ajettaessa Helsingistä Lahteen (110 km), kun oletetaan, että polttoaine palaa täydellisesti? Bensiini voidaan katsoa oktaaniksi (C8H18), jonka tiheys on 0,71 kg/l.
a) Otsonin vähentyminen ylemmissä
ilmakerroksissa on luonnon kannalta haitallinen ilmiö. Mitkä ovat
tärkeimmät kemialliset tekijät, jotka johtavat
otsonikatoon?
b) Otsoni on voimakas hapetin ja hapettaa jodidin
jodiksi:
Reaktioita voidaan käyttää otsonin määrän selville saamiseen. Menetelmässä vapautunut jodi titrataan natriumtiosulfaattiliuoksella:
Kuinka monta grammaa otsonia näyte sisälsi, kun titrauksessa käytettyä 0,15 M natriumtiosulfaattia kului 11,2 ml? Mitkä aineet hapettuvat ja mitkä pelkistyvät näissä reaktioissa?
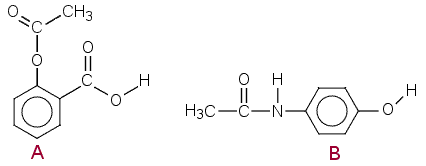
Kahden yleisesti käytetyn särkylääkkeen vaikuttavien aineiden rakenteet A ja B on esitetty oheisissa kuvissa. Kumpaakin yhdistettä voidaan valmistaa reaktion
avulla. Laadi lähtöaineiden X ja Y rakennekaavat, kun a) tuote on A, b) tuote on B. c) Laadi myös rakennekaavat reaktiotuotteille, jotka saadaan, kun yhdistettä A käsitellään väkevällä NaOH-liuoksella.
 |
Millä edellytyksillä orgaanisilla yhdisteillä voi esiintyä cis-trans-isomeriaa? Esitä rakennekaavat kaikille yhdisteille, joiden molekyylikaava on C2H2Cl2. Nimeä yhdisteet. Mitkä näistä yhdisteistä ovat polaarisia? Perustelu.
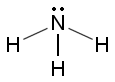
Mitä oheisen kuvan perusteella voit sanoa ammoniakkimolekyylin rakenteesta ja sen vaikutuksesta ammoniakin ominaisuuksiin? Miten ammoniakkia valmistetaan teollisesti, ja mihin sitä käytetään?
Tislaus on yleisesti käytetty erotusmenetelmä. Selvitä tislauksen periaate, kuvaa siinä tarvittavaa laitteistoa ja esitä jokin todellinen tilanne, johon menetelmää voidaan käyttää.
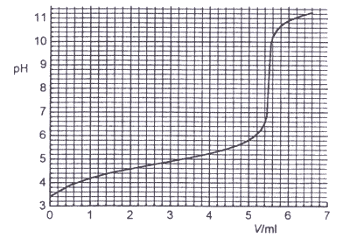
Kun erään yksiarvoisen hapon vesiliuoksesta
otettu 25,0 ml:n näyte neutraloitiin 0,10 M NaOH-liuoksella saatiin
oheinen titrauskäyrä. a) Mikä oli hapon konsentraatio
alkuperäisessä liuoksessa? b) Titrauksen päätepiste
todettiin suoran pH-mittauksen lisäksi myös
happo-emäsindikaattorin avulla. Mihin happo-emäsindikaattorien
toiminta perustuu, ja mitä seikkoja tuli ottaa huomioon indikaattorin
valinnassa? c) Määritä hapon happovakion arvo. d)
Työssä käytetty pH-mittari kalibroitiin liuoksella, jonka pH on
4,74. Liuos valmistettiin lisäämällä 0,10 M NaOH-liuosta
20,0 ml:aan 0,10 M etikkahappoa (Ka =